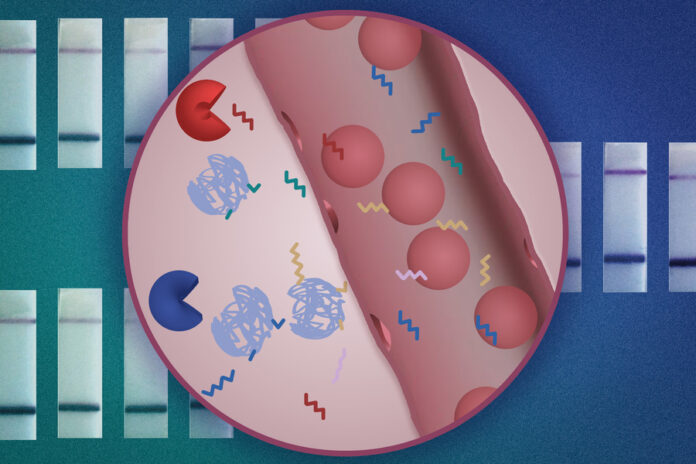
MIT mühendisleri, basit bir idrar testiyle kanserin erken teşhisini sağlayabilecek yeni bir nanoparçacık sensörü tasarladı. Birçok farklı kanserli proteini tespit edebilen sensörler, tümörün türünü veya tedaviye nasıl yanıt verdiğini ayırt etmek için de kullanılabilir.
Nanopartiküller, bir tümörle karşılaştıklarında idrarla atılan kısa DNA dizileri saçacak şekilde tasarlanmıştır. Bu DNA “barkodlarının” analiz edilmesi, belirli bir hastanın tümörünün ayırt edici özelliklerini ortaya çıkarabilir. Araştırmacılar testlerini, evde yapılan Covid testine benzer şekilde bir kağıt şeridi kullanılarak gerçekleştirilecek şekilde tasarladılar ve bu sayede mümkün olduğunca çok sayıda hasta için uygun fiyatlı ve erişilebilir olmasını umuyorlar.
John ve Dorothy Wilson Sağlık Bilimleri ve Teknolojisi Profesörü ve MIT’de Elektrik Mühendisliği ve Bilgisayar Bilimi Profesörü ve MIT’nin Koch Bütünleştirici Kanser Araştırmaları Enstitüsü ve Tıp Mühendisliği ve Bilimi Enstitüsü üyesi Sangeeta Bhatia “Teknolojiyi düşük ve orta kaynaklı ortamlarda kullanılabilir hale getirme bağlamında yenilik yapmaya çalışıyoruz. Bu tanıyı kâğıda dökmek, tanıyı demokratikleştirme ve bakım noktasında size hızlı bir yanıt verebilecek ucuz teknolojiler yaratma hedefimizin bir parçasıdır” diyor.
Fareler üzerinde yapılan testlerde araştırmacılar, sensörleri tümörlerde eksprese edilen beş farklı enzimin aktivitesini tespit etmek için kullanabileceklerini gösterdiler. Ayrıca, örnekleri analiz etmek için mikroakışkan bir cihaz kullanarak, yaklaşımlarının tek bir örnekte en az 46 diğer DNA barkodunu ayırt etmek için ölçeklendirilebileceğini gösterdiler.
Bhatia, bugün Nature Nanotechnology’de yayınlanan makalenin kıdemli yazarıdır. Eski bir MIT araştırma bilimcisi olan ve şu anda Boston Üniversitesi’nde biyomedikal mühendisliği yardımcı doçenti olarak görev yapan Liangliang Hao ise çalışmanın başyazarı.
DNA barkodları
Bhatia’nın laboratuvarı birkaç yıldır kanser teşhisinde kullanılabilecek “sentetik biyobelirteçler” geliştiriyor. Bu çalışma, bir hastanın kan örneğindeki proteinler veya dolaşımdaki tümör hücreleri gibi kanser biyobelirteçlerini tespit etme konseptine dayanıyor. Doğal olarak oluşan bu biyobelirteçler o kadar nadirdir ki, özellikle erken bir aşamada onları bulmak neredeyse imkansızdır, ancak sentetik biyobelirteçler küçük tümörlerde meydana gelen daha küçük ölçekli değişiklikleri büyütmek için kullanılabilir.
Bhatia önceki çalışmasında, hücre dışı matrisin proteinlerini keserek kanser hücrelerinin orijinal konumlarından kaçmalarına veya yeni konumlara yerleşmelerine yardımcı olan proteaz adı verilen enzimlerin aktivitesini tespit edebilen nanopartiküller oluşturdu. Nanopartiküller farklı proteazlar tarafından parçalanan peptitlerle kaplanmıştır ve bu peptitler kan dolaşımına salındıktan sonra konsantre edilebilir ve idrar örneğinde daha kolay tespit edilebilir.
Orijinal peptit biyobelirteçleri, kütle spektrometresi kullanılarak kütlelerindeki küçük mühendislik değişikliklerine göre tespit edilmek üzere tasarlanmıştır. Bu tür bir ekipman düşük kaynaklı ortamlarda bulunamayabilir, bu nedenle araştırmacılar CRISPR teknolojisi kullanılarak okunabilen DNA barkodlarını kullanarak daha kolay ve uygun maliyetle analiz edilebilecek sensörler geliştirmeye başladılar.
Bu yaklaşımın işe yaraması için araştırmacıların, dolaşımdaki DNA raportör barkodlarını kanda parçalanmaktan korumak için fosforotiyoat adı verilen kimyasal bir modifikasyon kullanmaları gerekiyordu. Bu modifikasyon, modern RNA aşılarının stabilitesini artırmak için zaten kullanılmış ve vücutta daha uzun süre hayatta kalmalarını sağlamıştır.
Peptit raportörlere benzer şekilde, her bir DNA barkodu, spesifik bir proteaz tarafından parçalanabilen bir bağlayıcı ile bir nanopartiküle bağlanır. Bu proteaz mevcutsa, DNA molekülü serbest kalır ve dolaşıma girerek sonunda idrara karışır. Bu çalışma için araştırmacılar iki farklı tipte nanopartikül kullandılar: biri, insanlarda kullanım için FDA onayı almış polimerlerden yapılmış bir partikül, diğeri ise bir tümör bölgesinde birikmek üzere tasarlanabilen bir antikor parçası olan bir “nanobody”.
Sensörler idrarda salgılandıktan sonra, numune Cas12a adı verilen bir CRISPR enzimi tarafından aktive edilen bir raportörü tanıyan bir kağıt şerit kullanılarak analiz edilebilir. Numunede belirli bir DNA barkodu bulunduğunda, Cas12a sinyali güçlendirir, böylece kağıt testinde koyu bir şerit olarak görülebilir.
Partiküller, her biri farklı bir proteaz aktivitesini tespit eden ve “çoğullanmış” algılamaya olanak tanıyan birçok farklı DNA barkodu taşıyacak şekilde tasarlanabilir. Daha fazla sayıda sensör kullanılması hem hassasiyet hem de özgüllükte artış sağlayarak testin tümör türlerini daha kolay ayırt etmesine olanak tanır.
Hastalık belirtileri
Farelerde yapılan testlerde araştırmacılar, beş DNA barkodundan oluşan bir panelin, ilk olarak akciğerlerde ortaya çıkan tümörleri, akciğerlere metastaz yapmış kolorektal kanser hücrelerinin oluşturduğu tümörlerden doğru bir şekilde ayırt edebildiğini gösterdi.
Hao, “Buradaki amacımız hastalık imzaları oluşturmak ve bu barkodlu panelleri sadece bir hastalığı okumak için değil, aynı zamanda bir hastalığı sınıflandırmak veya farklı kanser türlerini ayırt etmek için kullanıp kullanamayacağımızı görmek” diyor.
Araştırmacılar, insanlarda kullanım için beşten fazla barkod kullanmaları gerekebileceğini, çünkü hastaların tümörleri arasında çok fazla çeşitlilik olduğunu düşünüyorlar. Bu hedefe ulaşmaya yardımcı olmak için, Harvard Üniversitesi Profesörü Pardis Sabeti liderliğindeki MIT ve Harvard Broad Enstitüsü’ndeki araştırmacılarla birlikte çalışarak, bir örnekten 46 farklı DNA barkodunu okumak için kullanılabilecek bir mikroakışkan çip oluşturdular.
Bu tür bir test sadece kanseri tespit etmek için değil, aynı zamanda bir hastanın tümörünün tedaviye ne kadar iyi yanıt verdiğini ve tedaviden sonra nüksedip nüksetmediğini ölçmek için de kullanılabilir. Araştırmacılar şimdi parçacıkları insanlarda test etmek amacıyla daha da geliştirmek için çalışıyorlar. Bhatia tarafından kurulan bir şirket olan Glympse Bio, üriner tanı partiküllerinin daha önceki bir versiyonunun faz 1 klinik denemelerini gerçekleştirdi ve hastalarda güvenli olduklarını tespit etti.
Kaynak: MIT News